
Technologien
Das Aufkommen neuer pharmazeutischer Wirkstoffe führt zu einem Paradigmenwechsel in der Arzneimittelentwicklung. Eine der grössten Herausforderungen ist die aseptische Herstellung – eine entscheidende Voraussetzung für die Produktion von injizierbaren Arzneimitteln auf Proteinbasis –insbesondere mit Blick auf regulatorische Anforderungen. Fachleute von Helbling sind auf anspruchsvolle Lösungen spezialisiert, die regulatorische Compliance, Qualität, Skalierbarkeit und Effizienz nahtlos miteinander verbinden. Sie gestalten mit Kunden die Zukunft in diesem Bereich. Zum Tragen kommen dabei der Ansatz Quality by Design (QbD) und automatisierte Prozesse, die Vorteile des maschinellen Lernens nutzen.
Neue (Bio-)Pharmazeutika sowie Zell- und Gentherapien bieten innovative Wege zur Behandlung von Pathologien, zum Beispiel bei Krebs oder Autoimmunerkrankungen. Daraus resultiert ein Paradigmenwechsel in der Medikamentenentwicklung. Diese proteinbasierten injizierbaren Arzneimittel erfordern eine aseptische Herstellung, da eine Endsterilisation nicht möglich ist. Werden aseptische Produktionsanlagen konzipiert und in Betrieb genommen, müssen neue Vorschriften beachtet werden, etwa der EU-GMP-Annex 1 für die Herstellung steriler Arzneimittel. Viele Unternehmen stellt das vor Herausforderungen, die nicht mit gängigen Lösungen zu meistern sind.
Um die Vorschriften einzuhalten, gilt es, menschliche Eingriffe zu reduzieren sowie Chancen durch Automatisierung und Digitalisierung zu nutzen. Für die Planung aseptischer Anlagen sind Isolatoren zum Standard geworden. Diese basieren auf gefilterter Luft mit unidirektionalem Luftstrom in einem abgedichteten Schrank und bilden so eine Schutzbarriere. Damit verbunden ist hoher Investitions- und Betriebsaufwand. Hier setzt der ganzheitliche und systematische Designansatz Quality by Design (QbD) an. Er spart Kosten, verbessert die Ausbeute und ermöglicht früh einen Scale-up-Pfad.
Darüber hinaus bieten neue Technologien wie maschinelles Lernen (ML) neue Möglichkeiten für die Konstruktion und den Betrieb von aseptischen Linien. Das Potenzial von ML-Technologien zur Verbesserung der pharmazeutischen Herstellung ist zwar enorm, ihr Einsatz in stark regulierten Umgebungen erfordert jedoch erhebliches Know-how für dessen Validierung.
Helbling verfügt über Expertise in der Entwicklung komplexer Anlagen- und Automatisierungslösungen. Ein Fokus liegt dabei auf anspruchsvollen Anforderungen in regulierten Branchen wie etwa Pharma. Dies reicht von der Machbarkeitsanalyse einer kundenspezifischen aseptischen Linie über die Konzeptionierung potenzieller Lösungen und die effiziente Durchführung technischer Projekte bis hin zur Inbetriebnahme. Der hier angewandte systematische Ansatz, unterstützt von Natur aus QbD. Aktuelle Projekte zeigen die besondere Relevanz von QbD.
Im Folgenden wird zunächst die Anwendung von ML zur Automatisierung von Produktionsabläufen und zweitens die Automatisierung von Operationen in einem Isolator mittels Robotik diskutiert. Drittens wird eine Fallstudie von Helbling vorgestellt, mit der die Marktreife automatisierter aseptischer Zellen schneller als üblich erreicht werden kann.
1. Machine Learning (ML) in der Automatisierung von Abläufen
Beim Einsatz von ML in der aseptischen Fertigung gibt es bereits etablierte Anwendungsfälle: etwa die ML-basierte Identifizierung von Teilen, die Generierung von Greifpunkten durch Roboter oder die Qualitätskontrolle von Arbeitsschritten, die von einem Menschen oder Roboterarm ausgeführt werden. ML eröffnet auch spezifische Anwendungen innerhalb eines Isolators: beispielsweise die automatisierte visuelle Inspektion von Defekten in Primärbehältern während des sogenannten Fill-and-Finish-Prozessschritts oder von Roboterbewegungen.
Bei der Entwicklung eines ML-Modells müssen nicht nur rein technische Herausforderungen gelöst, sondern auch regulatorische Anforderungen erfüllt werden. Bisher gibt es keine spezifischen Vorgaben der Behörden an den Einsatz von KI in der pharmazeutischen Produktion. Regulatorische Rahmenbedingungen wie der EU-GMP-Annex 11 zu computergestützten Systemen und GAMP5 bieten jedoch eine allgemeine Orientierungshilfe: Durch den Einsatz computergestützter Systeme darf keine Verschlechterung der Produktqualität, der Prozesskontrolle, der Qualitätssicherung und keine Erhöhung des Gesamtrisikos des Prozesses entstehen.
Daher sollte die Entwicklung und Validierung eines KI/ML-Modells für eine kontrollierte Fertigungsumgebung einem systematischen Ansatz folgen. Relevante Faktoren des Modells sind hier Entscheidungsautonomie, Anpassungsfähigkeit an Veränderungen und angemessene Qualitätskontrollmassnahmen. Dabei braucht es einen End-to-End-Prozess in Bezug auf den gesamten Lebenszyklus eines KI/ML-Modells und die Validierung. Diese drei Punkte sind insbesondere relevant:
- Lebenszyklus von der Konzeption über die Entwicklung bis hin zum Betrieb/Überwachung (s. Abb. 1)
- Einsatz mit einem gewissen Mass an Kontrolle und Autonomie (s. Factbox & Tabelle 1 zum Reifegradmodell)
- Erforderliche Validierungsmassnahmen
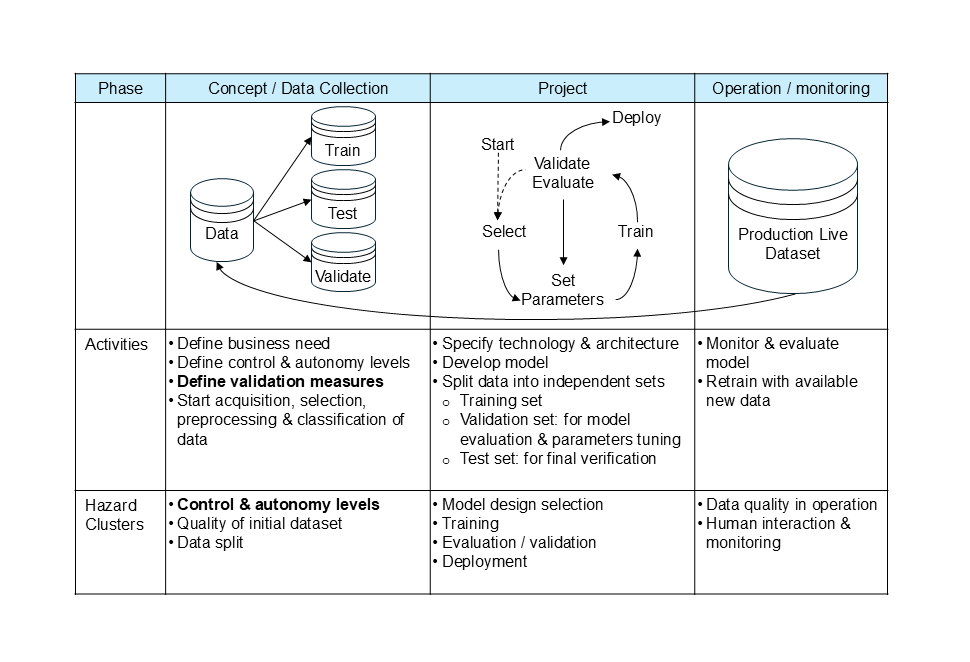
Anwendung des maschinellen Lernens
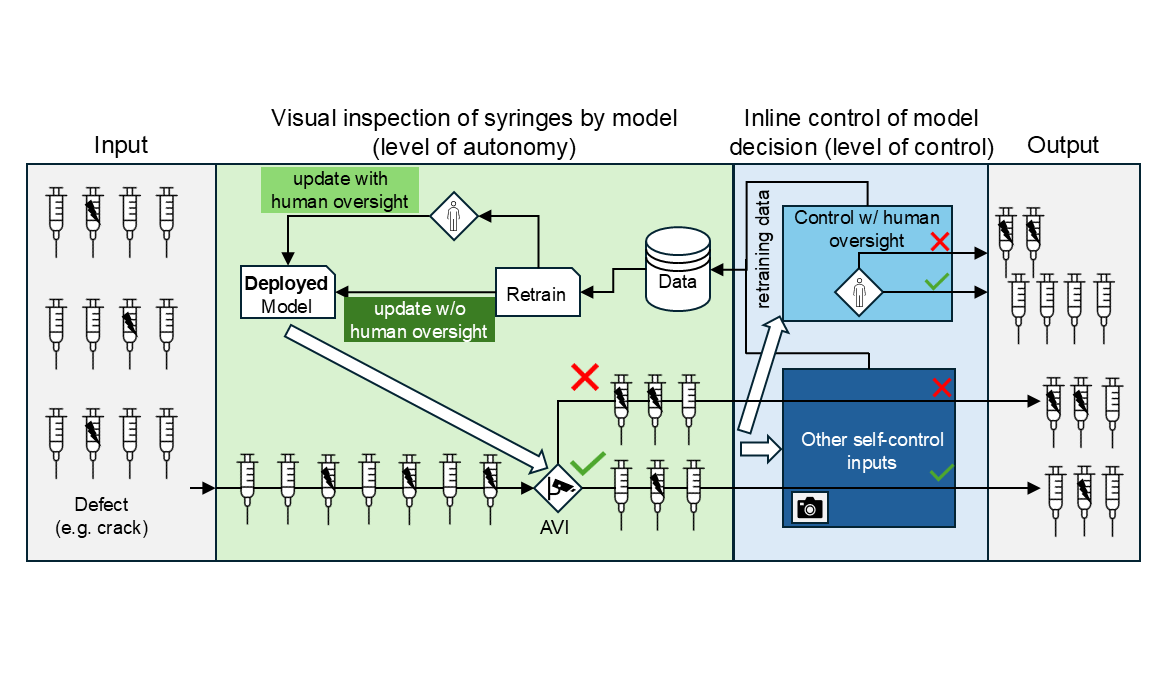
Im Rahmen der aseptischen Produktion kann ML bei der automatisierten visuellen Inspektion (AVI) unterstützen, etwa Risse und Partikel in Spritzen identifizieren (s. Abb. 2). Hier sind unterschiedliche Kontroll- und Autonomie-Level möglich.
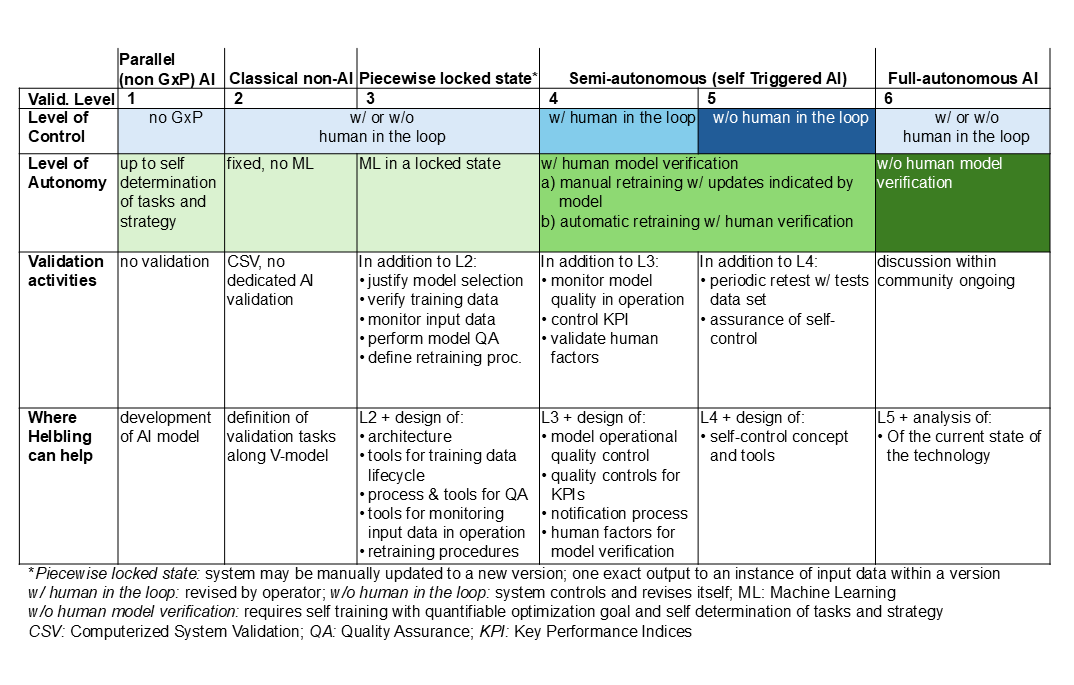
Den Zusammenhang zwischen Kontrollniveau und Modellautonomie und daraus resultierende Validierungsstufen verdeutlicht diese Tabelle, die sich am Reifegradmodell orientiert und zeigt, welche Unterstützung jeweils Helbling bieten kann.
Fachleute von Helbling haben Erfahrungen darin, KI- und ML-Lösungen in vielen Branchen umzusetzen. Das fängt bei der Konzeption und Erfassung von realen oder synthetischen Daten an, geht über die Identifizierung der Modellarchitektur und geht bis zu Validierungsaktivitäten. Ein Schlüsselelement für diese Anwendungen in einem regulierten pharmazeutischen Umfeld: Bei Anträgen in sehr frühem Stadium sind die Zulassungsbehörden offen für eine Diskussion und Helbling unterstützt Kunden im Dialog mit den Behörden.
2. Automatisierung von Operationen in einem Isolator mithilfe von Robotik
Bei manuell bedienten Isolatoren werden die Schritte von geschultem Personal mit hermetisch abgedichteten Handschuhen durchgeführt. Der Durchsatz eines manuellen Prozesses ist begrenzt. Auch die Variabilität der Bedienerbewegungen, das Berühren von Produktkontaktflächen mit Handschuhen und menschliches Versagen tragen zu einem höheren Kontaminationsrisiko bei. Auch für die Kleinserienproduktion hochwertiger Medikamente wird die Automatisierung immer wichtiger. Es unterstützt einen höheren Durchsatz, eine höhere Wiederholgenauigkeit und Prozessrückverfolgbarkeit.
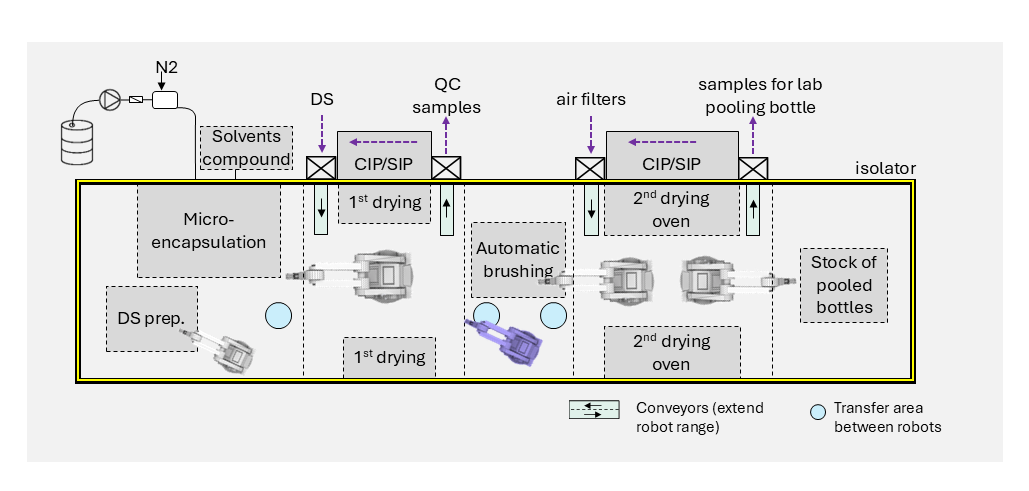
Bei kleinen Chargen werden Roboterarme bevorzugt, um die Anforderungen an die Prozessqualität zu erfüllen und gleichzeitig Flexibilität für verschiedene Primärverpackungsformate zu bieten. Bei der Wahl der richtigen Roboterlösung ist unter anderem Folgendes zu beachten:
- Zielkonflikt zwischen Geschwindigkeit und Flexibilität von 6-Achs-Robotern im Vergleich zu klassischen XY-Tischen
- Nutzlast
- Verträglichkeit mit den Reinigungs- und Sterilisationsprozessen (z.B. Wasserstoffperoxid-Dampf)
- Versiegeltes Design zur Minimierung der Partikelbildung durch Verschleiss
- Gestaltung der Robotertrajektorie, um die Einhaltung der First-Air-Prinzipien sicherzustellen
Der Prozess der Entwicklung und Herstellung von Medikamenten ist langwierig und komplex. Der Weg führt aus dem Labor über Kliniken, den Pilot-Status bis zur Kommerzialisierung, wobei sich der Herstellungsprozess nicht ändern sollte. Wer von Anfang an Skalierbarkeit und Modularität berücksichtigt, muss weniger investieren, um schneller eine Markteinführung zu erreichen.
3. Fallstudie: Ein dynamischer CFD-Ansatz für die Bewegung von Roboterarmen in First Air
Helbling hat in einer Fallstudie einen automatisierten aseptischen Abfüllprozess mit einem sechsachsigen Roboterarm in einem Isolator untersucht. Betrachtet wurde auch das Zusammenspiel zwischen Luftströmung, Reinraumeinrichtung und die Geschwindigkeit sowie Beschleunigung der Roboterbewegung. Dabei handelt es sich um Roboterarme mit einem hygienischen Design, das den Reinraumstandards GMP Grade A und ISO 14644-1 Klasse 5 entspricht. Entscheidend sind dabei die Prinzipien des schützenden Luftstroms, um Verunreinigungen in der Luft während des Fill-and-Finish-Schritts zu vermeiden. In Annex 1 wurde das sogenannte First-Air-Management als kritischer Aspekt eingeführt. Demnach muss ein kontinuierlicher, unidirektionaler und laminarer steriler Luftstrom über den kritischen Zonen sichergestellt werden.
Geht es um neue Anlagen oder neue Bedingungen im Umfeld, müssen Luftströmungsmuster für sterile Kernzonen im Rahmen von Rauchstudien visualisiert und validiert werden. Das ist in vielerlei Hinsicht aufwändig; Ziel ist eine von Beginn an fehlerfreie Produktion.
In der Fallstudie kamen digitale Zwillinge als Werkzeuge für die virtuelle Entwicklung und Inbetriebnahme zum Einsatz sowie Modelle im Bereich der Computergestützten Strömungsmechanik (Computational Fluid Mechanics / CFD). Diese helfen, die Luftströmungsdynamik zu verstehen und das Isolatordesign bereits vor den Qualifikationsstudien in der realen Welt zu optimieren. In einem ganzheitlichen Full-Stack-Ansatz wird CFD mit der Planung der Roboterbewegungen kombiniert.
Erkenntnisse aus der Fallstudie
In der Helbling-Fallstudie zeigt sich die Stärke dieses Ansatzes für das Design und die Optimierung komplexer robotischer aseptischer Anwendungen. Digitale Zwillinge helfen, die Effizienz, Sicherheit und Compliance von Prozessen zu verbessern.
Die Integration verschiedener Software-Tools in diesen Prozess erfordert die Kombination heterogener, nicht trivialer Schnittstellen. Das Verfahren ist iterativ und umfasst die Bewegungsplanung, die dynamische CFD-Simulation mit Komponenten in Bewegung und die Bahnoptimierung. Mit dynamischer CFD können Phänomene wie Wirbel und Turbulenzen erfasst werden, die möglicherweise ohne die Berücksichtigung von Bewegung nicht sichtbar sind.
Der Optimierungsprozess besteht unter anderem aus einer Bewegungsplanung, einer dynamischen CFD-Analyse sowie Optimierung der Roboterbewegung und des regelkonformen Designs.
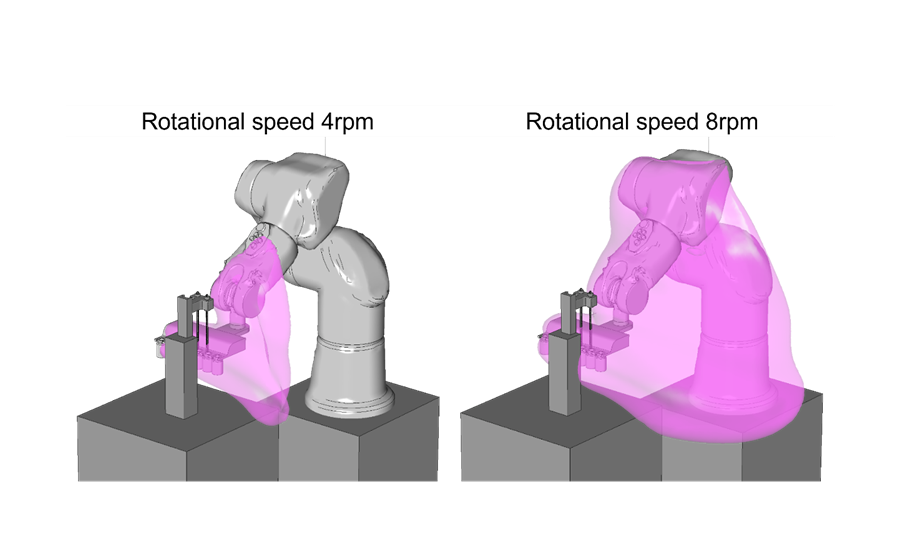
Die Fallstudie brachte zuvorderst drei Erkenntnisse:
- Das Tool hilft dabei, die optimale Roboterbahn zu finden, da die Bewegung die Stromlinien stark beeinflusst und turbulente kinetische Energie erzeugt.
- Das Tool trägt auch dazu bei, die Form und Aerodynamik der Ausrüstung optimal zu gestalten, da der Luftstrom schneller wird und möglicherweise umwälzt, wenn er über scharfe Kanten strömt.
- Der Einlass des Sterilluftverteilers muss den gesamten kritischen Arbeitsbereich abdecken, um die Entstehung von Wirbeln zu verhindern.
Das fachliche Know-how von Helbling in der industriellen Anwendung von CFD-Simulationen ist der Schlüssel, um Modelle am Sweet Spot zwischen Genauigkeit und Rechenzeit aufzubauen und ein leistungsfähiges Optimierungswerkzeug zu schaffen.
Zusammenfassung: QbD und Automation bilden die Basis für eine effiziente Produktion neuer Medikamente
Neue Regularien sowie Fortschritte bei neuen Therapieformen konfrontieren Pharmaunternehmen und ihre Partner mit einer Situation, in der Vorteile des Maschinellen Lernens und von Automatisierungslösungen immer relevanter werden. In diesem Zusammenhang kann Helbling seine Erfahrungen optimal einbringen. Dank des systematischen Quality-by-Design-Ansatzes kann sich der Mehrwert der Leistungsfähigkeit von KI-/ML-Modellen auch in regulierten Branchen entfalten. In Bezug auf Automatisierungen gilt es, den Prozessfokus beizubehalten, um Nutzen und Kosten in Einklang zu bringen. Schliesslich helfen dynamische CFD-Simulationen, bewegliche Roboterarme in die Produktion so zu integrieren, dass die Markteinführungszeit verkürzt und Kosten verringert werden.
Autoren: Alex Rüegg, René Hartnack, Simon Dössegger, Franck Robin
Hauptbild: Dall-e
[1] ISPE: AI Maturity Model for GxP Application: A Foundation for AI Validation, Nico Erdmann, Rolf Blumenthal, Ingo Baumann, Markus Kaufmann https://ispe.org/pharmaceutical-engineering/march-april-2022/ai-maturity-model-gxp-application-foundation-ai
[2] ISPE: Machine Learning Risk and Control Framework, Rolf Blumenthal, Nico Erdmann, Martin Heitmann, Anna-Liisa Lemettinen, Brandi Stockton https://ispe.org/pharmaceutical-engineering/january-february-2024/machine-learning-risk-and-control-framework?utm_campaign=2024%20PE&utm_content=278828325&utm_medium=social&utm_source=linkedin&hss_channel=lcp-214189



